近日,深圳大学物理与光电工程学院、生物医学光子学研究中心屈军乐教授课题组与乌克兰塔拉斯舍甫琴科基辅国立大学和乌克兰国家癌症研究所联合在阿尔茨海默症专业期刊《Alzheimer’sResearch & Therapy》(2-year Impact Factor: 6.982)上发表了题为《Near-infrared light reducesβ-amyloid-stimulatedmicroglial toxicity and enhances survival of neurons: Mechanisms of lighttherapy for Alzheimer's disease》的研究论文。Yurii V. Stepanov和IuliiaGolovynska博士为该论文的共同一作,屈军乐教授为该论文的通讯作者,深圳大学为第一完成单位。
光生物调控(photobiomodulation, PBM)利用低强度的光减缓阿尔兹海默症(Alzheimer’s disease, AD)等神经退行性疾病的恶化,降低皮质中淀粉样β(amyloid-β, Aβ)蛋白的水平。然而,光生物调控保护神经退行性疾病的细胞和分子机制的探索和研究仍处于早期阶段。其中,小胶质细胞通过引起慢性炎症,在AD的病理中发挥关键作用,所以调控小胶质细胞来抑制病症发展中的慢性炎症是治疗AD的重要思路。基于此,课题组研究并报道了利用808 nm近红外光进行光生物调控小胶质细胞氧化应激和细胞代谢激活的新成果。
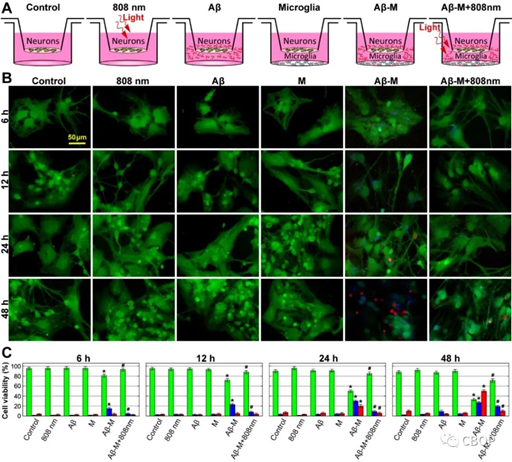
Figure 1. Increased neuron cell viability after NIR exposure in a co-culture with Aβ stimulated microglia.
在本研究中,从健康小鼠海马体提取出的小胶质细胞被寡聚体的Aβ(1-42)激活后,使用波长为808 nm的激光照射小胶质细胞5分钟(功率密度30 mW/cm2,照射剂量10 J/cm2)。为了全面评估PBM对小胶质细胞的影响,课题组测试了小胶质细胞的线粒体膜电位、活性氧(Reactive oxygen species, ROS)水平、细胞活力、凋亡和坏死,并采用标准方法测定吞噬细胞、一氧化氮和过氧化氢的产生和精氨酸酶和葡萄糖6-磷酸脱氢酶(glucose 6-phosphate dehydrogenase, G6PD)的活性,用ELISA法测定细胞因子、葡萄糖、乳酸和ATP等指标。结果发现,在受寡聚体Aβ激活的促炎症小胶质细胞中,PBM能有效诱导从糖酵解到线粒体活动的代谢转变。因此,抗炎型小胶质细胞(M2表型)数量增加,这意味着小胶质细胞的促炎因子的分泌减少和吞噬功能的激活。另外,PBM降低了Aβ诱导的G6PD的活性,这是一种调节戊糖磷酸通路速率的酶,它能激活烟酰胺腺嘌呤二核苷酸磷酸氧化酶(Nicotinamide adenine dinucleotide phosphate oxidase, NOX)进一步产生ROS。神经元的凋亡和数量减少是AD病的结果之一,为了探究PBM调控小胶质细胞是否会对神经元活性有促进作用,课题组在神经元与小胶质细胞的共培养模型中验证了PBM也可以通过调节被Aβ激活的小胶质细胞产生的ROS水平来有效减少神经元的凋亡。
Aβ处理的小胶质细胞会表现出代谢变化和炎症表型的转变,它通过激活NOX来刺激小胶质细胞生成高水平的ROS,但是PBM可以逆转这种Aβ诱导的变化,保护神经元免受损伤。利用近红外光调控被Aβ激活的小胶质细胞可能成为控制AD炎症发展的一种治疗策略。
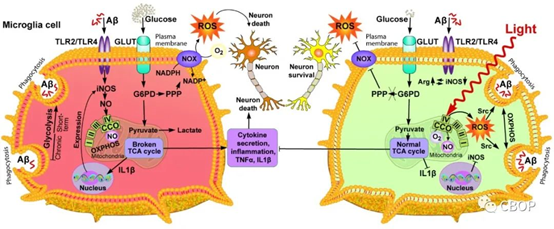
Figure 2. NIR light and Aβ are the metabolic regulators of microglial phenotype and function.
综上所述,本研究为基于近红外光的PBM在调节应激和小胶质细胞代谢中的作用提供了新的见解,并且为抑制小胶质细胞ROS产生和恢复代谢稳态提供了机制解释。可以预期,PBM治疗AD具有巨大的潜力。