近日,生物医学光子学研究中心在国际知名期刊《Advanced Functional Materials》(影响因子19.924,中科院JCR一区,TOP期刊)上发表题为“Multi-functional carbon dots for visualizing and modulating ROS-induced mitophagy in living cells”的研究论文,设计并制备一种可视化和调节活细胞中ROS诱导的线粒体自噬进程的多功能碳点。李灏专职研究员和郭嘉庆博士后为该论文的第一作者,宋军教授和严伟副教授为该论文的通讯作者,深圳大学为第一完成单位。
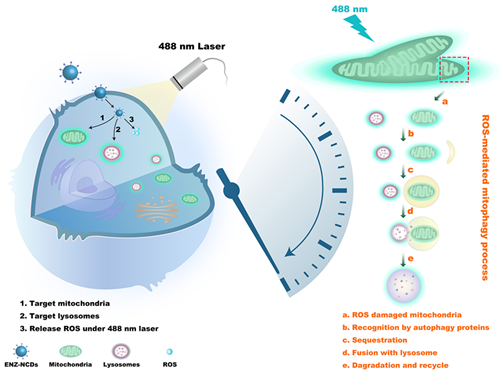
图1 ENZ-NCD细胞摄取、定位及相关应用。
活性氧(ROS)诱导的线粒体自噬与多种疾病有关。因此,可视化和调节ROS诱导的线粒体自噬进程对于理解线粒体自噬在细胞稳态、生理过程和发病机制中的作用至关重要。因此课题组设计并制备了一种既可以标记线粒体自噬相关细胞器又具有纳米酶催化性质的多功能氮掺杂碳点(ENZ-NCDs),ENZ-NCDs具有氧化还原酶特性,在488 nm激光调控下可以催化O2形成·O2−和1O2,同时ENZ-NCDs作为荧光探针,可以通过能量依赖转运(网格蛋白介导的和小泡介导的内吞作用)和自由扩散进入活细胞体内靶向线粒体和溶酶体。
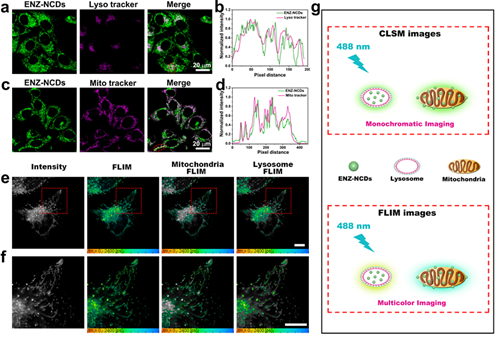
图2 ENZ-NCDs与商业亚细胞器染料的共定位分析,以及ENZ-NCDs处理后的HeLa细胞的FLIM双色成像。
此外,由于ENZ-NCDs靶向线粒体和溶酶体后荧光寿命发生变化,基于FLIM成像技术首次利用单一探针,实现了在单一激发波长下的细胞器多色成像。同时靶向细胞器的ENZ-NCDs,在488 nm激光照射下产生的ROS可增加相关线粒体自噬蛋白(Parkin、PINK1、LC3-II和p62)的表达,从而诱导PINK1/Parkin通路介导的线粒体自噬。更重要的是基于FLIM成像技术,利用靶向溶酶体和线粒体的ENZ-NCDs荧光寿命比值(τlysosomes/τmitochondria)的实时变化,可以进一步证明线粒体自噬的发生并能够实时的反映出ROS诱导的线粒体自噬的动力学信息。
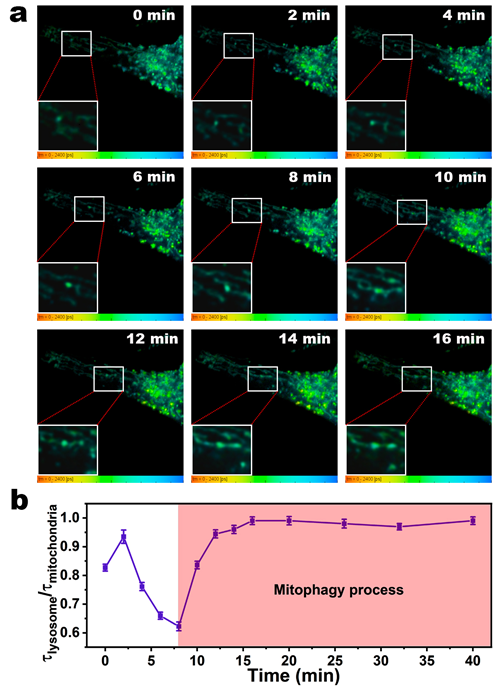
图3 ENZ-NCDs对活细胞线粒体自噬过程的实时FLIM成像研究。
该研究成果为后续制备适合FLIM多色成像的新型探针提供了新的思路。更重要的是,制备的ENZ-NCDs可以作为一种新型探针,用于未来线粒体自噬进程的实时监测以及量化ROS引起的线粒体损伤和ROS诱导的线粒体自噬相关疾病的研究。
该研究得到了国家自然科学基金项目、中国博士后基金项目、广东省教育厅基金和深圳市基础研究计划项目的支持。
论文原文链接:https://doi.org/10.1002/adfm.202212141